
Ванадий — металл, простое химическое вещество,  элемент таблицы Менделеева. Впервые был открыт мексиканским химиком Андресом Дель Рио в 1801-м году. Но перед европейскими учеными свое открытие он отстоять не смог, и вторично металл был открыт спустя 30 лет шведом Нильсом Сефстрёмом. Название новый элемент получил по имени богини любви и красоты Ванадис из-за того, что на воздухе на поверхности металла образуется красивая пленка из разноцветных оксидов.
элемент таблицы Менделеева. Впервые был открыт мексиканским химиком Андресом Дель Рио в 1801-м году. Но перед европейскими учеными свое открытие он отстоять не смог, и вторично металл был открыт спустя 30 лет шведом Нильсом Сефстрёмом. Название новый элемент получил по имени богини любви и красоты Ванадис из-за того, что на воздухе на поверхности металла образуется красивая пленка из разноцветных оксидов.
Ванадия на планете достаточно много, но он крайне рассеян и не встречается в чистом виде. В очень небольших количествах входит в состав более чем сорока минералов. Больше всего его в роскоэлите, карнотите и ванадините. Его относительно много также в патроните, деклуазите. Часто встречается в качестве сопутствующего элемента в рудах, содержащих другие металлы. Добывают его большей частью из железных, медно-свинцово-цинковых, титаномагнетитовых, урановых руд, сланцев и т.п. Ванадий выделяют из отходов после добычи основного металла. Руды, содержащие 1% ванадия, считаются очень богатыми. Оправдана добыча из сырья, в котором элемента всего 0,1%.
Это интересно
Ванадий накапливается некоторыми видами морских организмов — голотуриями и асцидиями, причем в значительных количествах. Японцы решили использовать эту особенность. Они выращивают на подводных плантациях асцидий вида Pyura chilensis, больше всего похожих на камни, с очень твердой внешней оболочкой серого цвета. Потом их сжигают и из золы добывают ванадий. Содержание металла в золе может достигать 5% — это много больше, чем в большинстве ванадиесодержащих руд.
 | 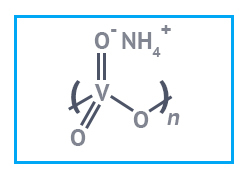 |
| Государственный стандартный образец состава раствора ионов «Ванадий (V)» | Аммоний ванадиевокислый мета |
Свойства
Светло-серый, серебристый металл, внешне напоминающий сталь. Пластичный и ковкий, легко обрабатывемый давлением и прокатом. При нагревании выше +300 °С теряет пластичность, становится хрупким, поэтому резать и сверлить его можно только в определенных условиях. Очень тугоплавкий, температура плавления +1887 °C. На воздухе окисляется, образуя пленку из оксидов разных цветов.
В химических реакциях малоактивен, устойчив к воздействию воды, в том числе морской, неконцентрированных кислот и щелочей. Образует несколько оксидов с разной валентностью. При определенных условиях взаимодействует с кислородом, водородом, азотом, углеродом, галогенами. С помощью различных химических преобразований получают соли ванадиевой кислоты, называемые ванадатами.
Ванадий в качестве микроэлемента участвует в метаболизме живых существ, включая человека, но его избыток вреден, так как соединения реактива ядовиты. Острое отравление вызывает воспаление слизистых дыхательных путей, глаз, кожи. В дальнейшем могут развиться лейкемия, анемия, аллергии, кожные заболевания, нарушения обменных процессов в организме.
Применение
- Легирующая добавка для получения биметаллов; жаростойких, ударопрочных, стойких к коррозии, износостойких, но легких сталей для авиационной, космической, машиностроительной и военной промышленности; для выпуска высококачественных ручных и механизированных инструментов. Легируют ванадием также алюминий, медь, никель, титан, тантал, ниобий, хром и даже золото, получая прочные и химически стойкие материалы для разных отраслей. Например, сплав никеля и ванадия используется для изготовления лабораторной посуды.
- В производстве анодов для мощных
 литиевых аккумуляторов (пятиокись ванадия); катодов для химических батарей.
литиевых аккумуляторов (пятиокись ванадия); катодов для химических батарей. - Для изготовления труб ТВЭЛов ядерных атомно-водородных реакторов на быстрых нейтронах.
- В качестве пигментов для производства красок, цветного стекла, керамики.
- Для получения анилиновых красителей и индиго, необходимых для окрашивания тканей из шелка и хлопка.
- Катализатор в синтезе серной кислоты. Ванадий значительно дешевле платины, которую применяли для этих целей раньше.
- Катализатор в процессах крекинга нефти, производства уксусной кислоты, в других промышленных синтезах.
- Хлорид ванадия используется в термическом разложении воды.
- В сельском хозяйстве применяются ядохимикаты и микроудобрения на основе ванадия.
- Для производства компонентов компьютеров, электронных и запоминающих устройств.
- В медицине, военном деле.